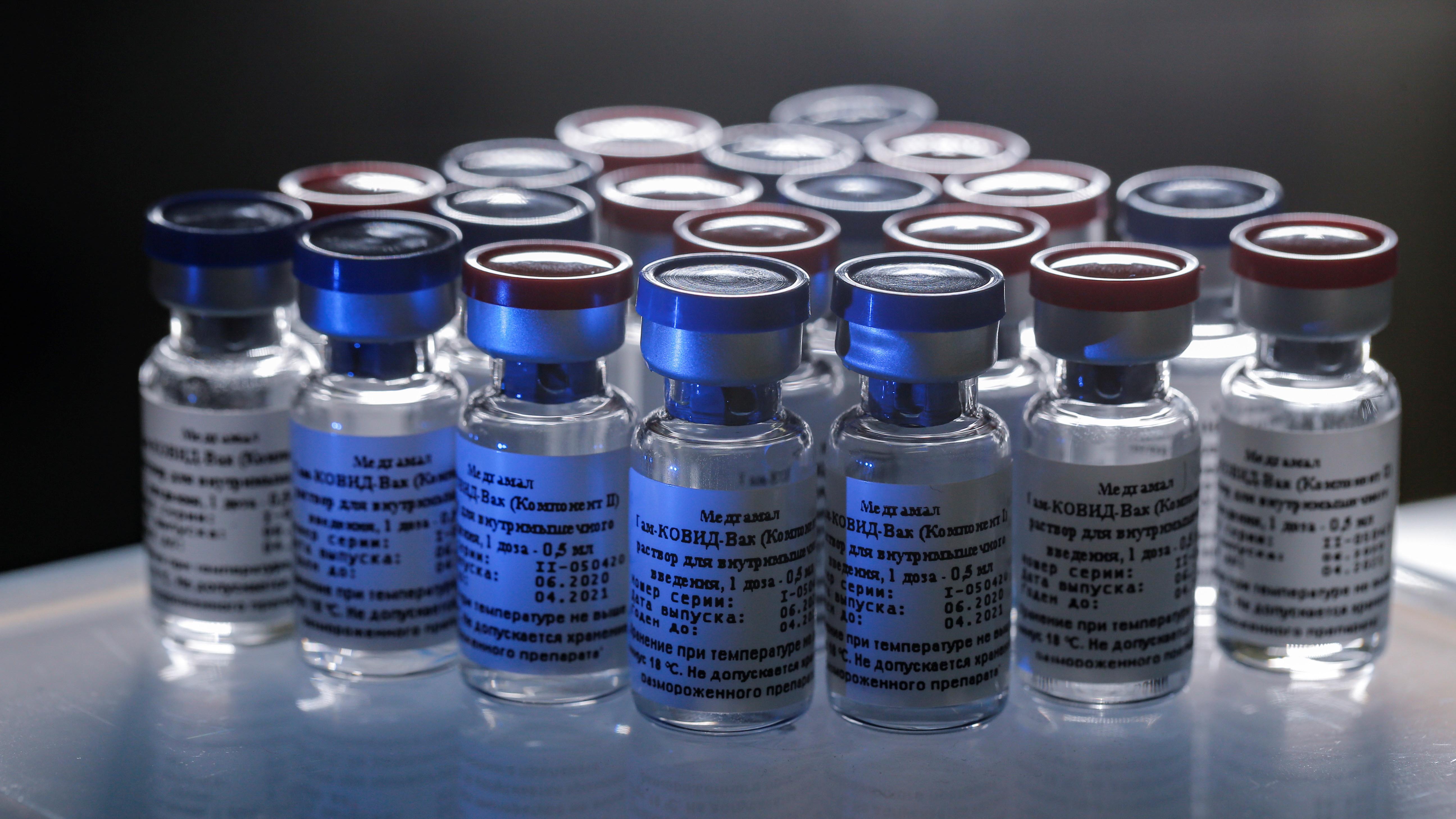
Este jueves, los pacientes de UC Davis Health se convirtieron en los primeros e en el área de Sacramento en recibir una vacuna candidata para COVID-19, que es parte de un importante ensayo clínico en el que participaron 30, 000 participantes en todo el mundo.
Según un comunicado de UC Davis, las seis personas que recibieron la inyección forman parte de un estudio de última etapa que inscribirá a unos 200 participantes a través del programa de ensayos clínicos de UC Davis Health.
"Estoy emocionado de poder tener la oportunidad de ayudar al mundo a enfrentar esta pandemia", dijo Lucas Solano, de 27 años, quien se inscribió en el ensayo hace unos días y recibió la inyección el jueves. "Es emocionante ser una de las personas que esencialmente tomaría la iniciativa y sería útil si esta vacuna fuera aprobada y distribuida en todo el mundo".
El ensayo dirigido por Pfizer Inc. y BioNTech está en curso y aún acepta participantes.
El ensayo de investigación, conocido como estudio de fase 2/3, busca determinar la eficacia y los efectos secundarios de un único candidato de ARN mensajero modificado con nucleósido (ARN mod) del programa de vacunas basadas en ARNm BNT162 de las compañías farmacéuticas.
La vacuna candidata ha sido sometida a una evaluación rigurosa en los Estados Unidos y Alemania y anteriormente ha mostrado resultados positivos significativos, según Pfizer.
UC Davis Health, que incluye el único centro médico académico de Sacramento, es uno de los 120 sitios que participan en el ensayo.
El gigante farmacéutico Pfizer, que se asoció con BioNTech más pequeño de Alemania, seleccionó sitios de estudio de vacunas conocidos por su experiencia de investigación de clase mundial, infraestructura y concentraciones cercanas de casos de COVID-19 positivos conocidos y anticipados.
UC Davis ha desempeñado un papel activo en la búsqueda de soluciones para combatir la enfermedad por coronavirus desde que los proveedores del Centro Médico de UC Davis diagnosticaron y trataron el primer caso aparente de COVID-19 en los Estados Unidos adquirido por propagación comunitaria en febrero.
“Este es un día histórico para la Facultad de Medicina de UC Davis”, dijo Allison Brashear, decana de la facultad de medicina. "Este es un cambio de juego para nuestra capacidad de comenzar a luchar contra la pandemia".
El ensayo está diseñado como una vacuna en investigación candidata a placebo, aleatorizada y ciega al observador para obtener los datos de seguridad, respuesta inmune y eficacia necesarios para la revisión regulatoria.
La vacuna es una de las varias que se están desarrollando en todo el mundo, a una velocidad récord, debido a la necesidad de detener la propagación del virus que ha matado a más de 170, 000 personas en los Estados Unidos, incluidas unas 12,000 en California.
"Impulsar un estudio de vacunación como este, dado el clima actual con el virus es extremadamente grande", dijo Chris Kain, una enfermera de UC Davis Health que ayuda a supervisar los ensayos clínicos y coordina con varios departamentos antes de que los primeros participantes del jueves recibieran sus vacunas. "Ha sido increíble ver a todos los equipos trabajando juntos".
UC Davis Health presta servicios en una región geográfica poblada por múltiples razas y etnias, lo que aumenta las posibilidades de identificar candidatos para ensayos clínicos de orígenes más diversos, en comparación con otras comunidades de los Estados Unidos. Los latinos y los negros se han visto afectados de manera desproporcionada por el virus y se les anima a inscribirse en el estudio. Se anima a participar a los trabajadores sanitarios y a quienes trabajan en entornos con un gran volumen de clientes, como las tiendas de abarrotes.
El objetivo principal del ensayo es prevenir el COVID-19 en aquellos que no han sido infectados por el SARS-CoV-2 antes de la inmunización y prevenir el COVID-19 independientemente de si los participantes han sido previamente infectados por el SARS-CoV-2. Un objetivo secundario es prevenir el COVID-19 grave en esos grupos.
Si el éxito de la vacuna candidata continúa, Pfizer y su socio europeo BioNTech han declarado que están en camino de buscar una revisión regulatoria a partir de octubre. Si se obtiene la autorización o aprobación regulatoria, las empresas planean suministrar hasta 100 millones de dosis para fines de 2020 y aproximadamente 1,300 millones de dosis para fines de 2021.